实时动态,深度解析,把握行业脉搏
实时动态,深度解析,把握行业脉搏
来源|时代商学院
作者|黄有谦
编辑|陈欣欣
一、市场表现
3 1月,上证综指(.SH)下跌6.07%,深成指(.SZ)下跌9.94%,沪深300指数(.SH)下降 7.@ >84%。
按照申万二级分类,医疗器械(.SI)下跌13.83%,跑输上证综指7.@>76个百分点和深成指3.@ >89 个百分点,沪深 300 5.99 个百分点。
与一级医药生物细分行业其他行业指数相比,除医疗器械外,医药业务(.SI)上涨11.28%,中药II(.SI)上涨1 1. 4.75%,医疗服务 (.SI) 上涨 1.1%,化学制药 (.SI) 上涨 0.66%。
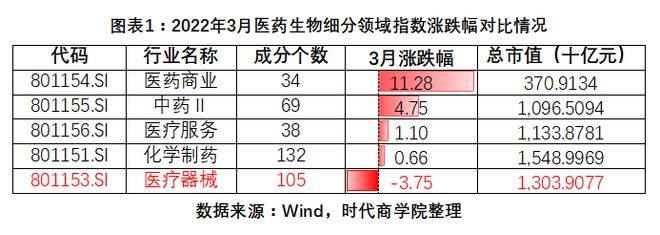
具体而言,A股市场105家医疗器械上市公司中,涨幅前五的分别是华康医疗(.SZ)、明德生物(.SZ)、九安医疗(.SZ)、爱鹏医疗(.SZ) .SZ)、东方生物(.SH),3月累计涨幅30.35%、21.2%、17.@>75%、14. 68%,13.42%。
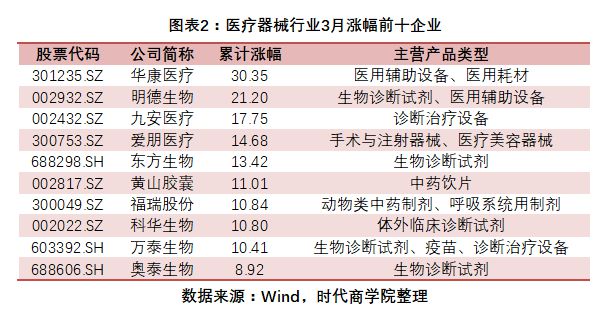
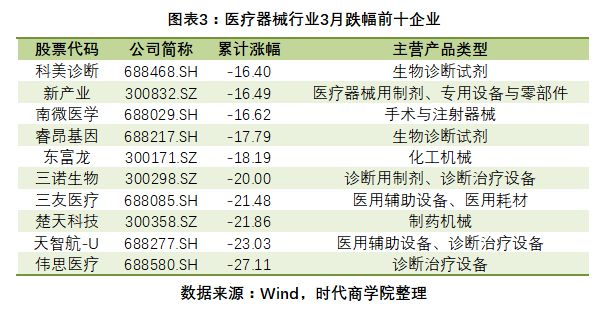
伟思医疗(.SH)、天之航(.SH)、楚天科技(.SZ)、三友医疗(.SH)、三诺生物(.SZ)分别为-27.@>11%,- 23.03%、-21.86%、-21.48%、-20%跌幅进入前五。
值得注意的是,2月份,三友医疗以-10.21%的跌幅位居当月前十榜单的第四位。本月公司股价继续下跌。累计下降也排名第四。
二、行业政策亮点
1.管理办法修订版]
3月22日,现场监管总局印发修订后的《医疗器械生产监督管理办法》和《医疗器械经营监督管理办法》,自2022年5月1日起施行。
医疗器械安全与人们的身体健康息息相关。两项措施严格落实“四个最严”要求,贯彻落实《医疗器械监督管理条例》,全面落实医疗器械注册人备案制度。优化行政许可流程,强化监督检查措施,改进监督检查方式,压实企业主体责任,进一步加大违法处罚力度。

执行最严格的监管要求。加强对医疗器械注册人的监督管理,明确注册人与委托生产企业的责任,将委托生产管理的相关要求纳入质量管理体系,进一步完善检查职责、检查方式、结果处置、医疗器械生产调查。取证和其他监管要求。
完善业务流程销售、运输、仓储等环节的管理要求,细化进货检验、销售记录等追溯管理相关规定,加强注册人、备案人销售其注册商标的质量安全。提起医疗器械责任。 (国家食品药品监督管理局)
2.【国家食品药品监督管理局:射频治疗仪、“水光针”等作为医疗器械监管】
为进一步深化医疗器械审评审批制度改革。 3月30日,国家药品监督管理局发布关于调整《医疗器械分类目录》部分内容的公告(以下简称《公告》),《医疗器械分类目录》涉及的27种医疗器械目录”。调整了“目录”的内容。
其中,本次公布的《医疗器械分类目录》调整内容包括部分医美产品。 《公告》明确以下医美产品按医疗器械管理。自实施之日起,根据《医疗器械监督管理条例》的规定,未依法取得医疗器械注册证的产品不得生产、进口和销售。详情如下:
1.射频治疗仪,射频皮肤治疗仪,用于治疗皮肤松弛,减少皮肤皱纹,收缩毛孔,收紧和增强皮肤组织,或治疗痤疮,疤痕,或减脂(脂肪软化或分解)等,按照第三类医疗器械明确规定。
2. 面部植入物、面部提升器和面部锥形提升器植入面部组织,以提升下垂组织并纠正皱纹,均符合 III 类医疗器械法规。
3.注射用透明质酸钠溶液用于注射到真皮层,主要是通过所含的透明质酸钠等物质的保湿补水作用来改善皮肤状况。符合III类医疗器械监管。
《公告》指出,自2024年4月1日起,未经依法取得医疗器械注册证的,不得生产、进口和销售射频治疗仪、射频皮肤治疗仪等产品;其余产品的实施日期相同。公告的发布日期。 (国家食品药品监督管理局)
3.【国家食品药品监督管理局关于印发《禁止委托生产医疗器械目录》的通知】
3月11日,为加强医疗器械生产监管,确保医疗器械安全有效,国家食品药品监督管理总局发布了《禁止委托生产医疗器械目录》。 《目录》自2022年5月1日起施行,原国家食品药品监督管理局《关于印发禁止委托生产医疗器械目录的通知》(2014年第18号)同时废止.
《目录》规定了植入式心脏起搏器、植入式心脏收缩调节器、植入式循环辅助装置等有源植入式器械;
硬脑膜(脊椎)膜贴片(不含动物源性材料的产品除外)、颅内支架系统、颅内动脉瘤血流导管、心血管植入物(外周血管支架、腔静脉滤器、心血管栓塞装置)等被动植入装置除外)、塑料填充材料、塑料注射填充物、乳房植入物、组织工程支架材料(不含同种异体或动物源性材料的产品除外)、可吸收性外科防护胶粘敷料等;
其他异体植入性医疗器械和直接从动物组织等中获取的植入性医疗器械,禁止委托生产。 (国家食品药品监督管理局)
4.【19款新型冠状病毒抗原检测试剂获批,其中广东4款】

3月23日,国家食品药品监督管理总局批复了2个新型冠状病毒抗原检测试剂产品。截至3月23日,国家食品药品监督管理局已批准19款新型冠状病毒抗原检测试剂产品医疗信息系统,其中广东省4款。
为保障广东省新型冠状病毒抗原检测试剂供应,广东省药品监督管理局集中全系统检查审批资源,全力支持全省抗原检测试剂注册审批工作.
3月23日,分别获得国家药品监督管理局颁发的新冠病毒抗原检测试剂注册证,全省现有抗原试剂证书持有者增至4家,有效保障了新冠病毒抗原在我省检测试剂市场供应。
下一步,广东省药监局将继续积极推进保障抗原检测试剂安全和促产工作,全力扩大产能;继续加强对研发注册环节的指导,做好注册产品注册质量管理体系的验证工作,推动更多抗原检测试剂产品在全省注册上市。 (广东省食品药品监督管理局)
5.【江苏扬州组织销毁收缴物资】
近日,江苏省食品药品监督管理局扬州检验分局将设立两年度,将350箱非法生产的近百万元的药用机械化产品运往邗江区杨庙镇进行无害化销毁此次行动主要采取了三项措施:
市局加强对没收物资的管理,建立健全没收物资台账,实行专人、专库集中管理,防止丢失;确保销毁材料的公司名称、品种信息、批号和数量,确保没有错误或遗漏。
市局加强与省局相关部门、生态环境部门的沟通,提前向省局计财处、稽查处报告销毁程序,并获得专业指导;安排人员参观分公司所在地生态环境 环保部门进行面对面交流,并为政府部门开设危废处置专项账户。
监管部门将联系无害化处理公司,签订销毁合同,明确双方的责任和义务,确定没收物资的运输和销毁方式,确保没收物资不丢失、不被污染在销毁过程中。
下一步,江苏省食品药品监督管理局扬州检验分局将继续深入贯彻落实防疫要求,结合药品安全专项整治和“立健2022”专项行动,进一步加大对药品机械化领域违法违规行为的查处力度。为全市医药产业高质量发展和人民群众安全有效用药保驾护航。 (中国食品药品网)
6.【吉林延边部署医疗器械质量安全隐患排查整改】
近日,吉林省延边朝鲜族自治州市场监督管理局对国家2022年医疗器械安全监管工作作出部署,努力实现深入排查隐患,有效防范风险的目标严格落实主体责任,严厉打击违法违规行为,全面提升质量管理水平。
本次排查整改工作重点针对疫情防控医疗器械、国家或省级集中采购中选产品、无菌和植入式医疗器械产品,发现了诸多问题和社会关切。高水平医疗器械产品生产经营企业、医疗器械记录仪委托生产、医疗器械经营许可(备案)及使用、医疗器械网络销售等环节。
排查整改工作明确。要通过多种渠道收集安全风险信息,通过风险咨询及时研判,以问题为导向,多维度了解、掌握、分析和判断风险。要加大对投诉举报和舆论问题的处理力度,鼓励有奖举报,从投诉举报中挖掘有价值的违法违规线索。要加强与公安、卫生、工信、医保、网信等部门的工作联系,形成监管合力,共同推动提高隐患排查整改和监管水平。从多个方面和维度对医疗器械进行分析。 (中国医学报)
7.@>【国家医保局:新冠抗原试剂盒纳入医保】
新冠抗原试剂盒已经上架十天,经过快速审批,经过积极降价、集中采购等一系列动作,迅速进入医保。 3月21日,国家医保局发布《关于切实做好当前疫情防控医疗保障工作的通知》(以下简称《通知》)。
《通知》提出,将新型冠状病毒抗原检测试剂及相应检测项目按程序暂纳入本省基本医疗保险医疗服务项目目录。参保人在定点基层医疗机构发生的相关费用按照统筹区现行规定支付,购买检测试剂的费用可使用个人账户支付。
各省级医保部门参照《国家医保局办公厅关于地方拟定的新冠病毒临时抗原检测项目及有关事项的意见的函》(医保办函[2022]11号),继续规范和优化公立医疗机构提供的COVID-19抗原检测服务的定价政策。
各地药品集中采购机构要做好新型冠状病毒抗原检测试剂网上采购工作,积极推进网上采购,依托全国统一医保信息平台进行信息共享。同时,加强计算和监测,协调推进价格、采购、支付和信息系统改造。 (赛博蓝仪器)
7.6@>经纪人观察研究报告
1.【新冠病毒抗原检测市场已打开,检测试剂盒全产业链将受益】
2022年3月11日,国务院新冠联防联控综合组印发《关于印发新冠病毒抗原检测应用方案(试行)的通知》,为进一步优化新冠病毒检测战略和服务。为适应疫情防控需要,在核酸检测的基础上,将增加抗原检测作为补充。
2022年2月以来,全国多地出现新冠疫情,新增病例多,城市疫情防控难度加大。抗原检测以其速度、便捷等优势,可以加快封闭区域居民的大规模筛查,降低政府疫情防控成本,缩短相关疫区隔离时间。
因此,抗原检测在中国具有潜在的蓝海空间。虽然新冠检测的主流方法和金标准仍将是核酸检测,但不可否认,抗原检测作为核酸检测的补充意义重大。
目前国内共有5款新冠抗原快速检测POC专业版试剂盒产品获批,需要专业人员操作。可在药店、网络销售平台等渠道购买的家庭自测版产品尚未获批。新政策的出台有望加快家庭版的审批。获得批准的制造商有望获得先发优势,并率先获得大量收入。随着抗原检测方法的逐步落地,相关试剂盒及上下游产业链将直接受益。 (开源证券)
2.【联合集中采购逐步实施,非中选品种支付机制调整】
2022年3月30日,国家医保局办公室、国家卫健委办公厅联合印发《关于集中采购使用高值医用耗材(人工关节)的意见》国家组织的配套措施”。结合人工联合采购、配送、使用和伴随服务的特点,集中采购平台与互联网联动。 、医保基金预缴、医保缴费政策、医疗服务价格调整、医疗机构激励约束等提出新的意见和措施,保障人工关节评选结果的顺利实施。
本文件明确,非中选人工关节产品中包含中选产品成分的,将按照选择价格挂网,其他成分可根据实际成交价格合理设置。对部分产品在网上上市进行限制,引导相关企业逐步将价格调整至合理水平。
文件要求,医疗机构与中选企业签订采购协议后,应按不低于年度协议采购金额30%的比例向医疗机构预缴医保基金。医疗机构应及时与企业结算货款,结算时间不得超过耗材使用时的次月末。并在落实医疗机构货款支付主体责任的前提下,鼓励医保资金直接与医药企业结算。未来,医保资金结算效率和企业贷款结算有望进一步提升。
医保局人工关节采购政策文件实施后,国内大部分人工关节产品将完成价格调整。产品终端价格的下降将直接压缩过去分销模式中人为的高利润率,但厂商有望保持合理的利润率,有利于规范耗材的采购和使用,改善行业生态。 (国金证券)
3.【行业迎来发展拐点,国产替代大有可为】
科研+产业两轮驱动,未来增长可期。我国生物科研试剂的下游是科研机构和医药行业用户,其研发投入不断加大,促进了生物试剂市场空间的打开。 2015年至2020年,我国生命科学投资年均复合增长率高达13.0@>3%。随着经济的蓬勃发展,配套试剂的需求稳步增长。
新冠疫情带来发展机遇,国产替代时机已到。 2020 年的 COVID-19 疫情限制了全球供应链。国内企业抓住机遇,创新研发新冠相关产品,业绩大幅增长,市场占有率不断提升。此外,国内厂商在某些领域的技术开发和定制服务方面具有很强的竞争力。我们认为,国内企业可以通过灵活的定价策略与海外企业竞争,促进进口替代的加速。
我们相信,在我国科研投入和下游生物医药产业持续高景气的背景下,我国生命科学试剂产业将保持高速增长。现阶段,行业本土化率仍较低。企业不断加大研发和技术升级,未来国产替代空间广阔。 (财新证券)
4.【《方舱方舱医院设置管理规范》出台,医疗设备、医院建设、医院感染控制相关股票有望受益】
新冠确诊病例短期内呈上升趋势,方舱医院建设势在必行。 3月22日,国家卫健委印发《方舱医院设置管理规范》,对方舱医院选址、三区两通道设置、医疗机构配置等方面进行了详细指导。人员,以及污水和废物的处理。 .
建造临时医院,以快速治疗无症状或轻度 COVID-19 患者。国务院联防联控机制综合组要求各省根据疫情情况,建设或拿出方舱医院建设方案,确保各省至少有2-3个方舱医院。目前,全国已建或在建方舱医院33家,分布在12个省19个城市,其中已建20家,在建13家,合计3. 50,000 张床位。
从长远来看,医疗设备、医院建设和医院感染控制有望受益。 2020年5月,国家发展改革委、国家卫健委、国家中医药管理局联合印发《公共卫生防治能力建设规划》,开启我国新型医疗基础设施建设。我们预计“十四五”期间,包括三级医院新建改扩建、千县工程、中医生育保险、方舱医院建设等,将为市场带来百亿增量。 . (开源证券)
5.【手术机器人方兴未艾,迎来行业布局底部机会】
手术机器人能有效解决临床需求,行业处于早期阶段,未来增长空间百亿。据Frost&data,2020年全球市场规模约为83亿美元,欧美市场占比76.5%,中国仅占5.1%。渗透率还有很大的提升空间。 2020年国内手术机器人市场基数4亿美元,预计到2026年达到38亿美元,约合人民币242亿元,年复合增长率高达44. 3%。
政策导向+医保扶持+产品实力提升+5G远程创新技术推动行业繁荣。 2015年以来,国家大力支持创新医疗器械发展,医疗机器人等高性能诊疗设备被列入重点支持方向。鉴于手术机器人成本高昂,北京、上海等地相继推出手术机器人纳入医保,大大降低了手术机器人的应用门槛。我们认为这样的地方政策未来在其他地区推广的可能性更大。
腹腔镜和骨科手术机器人引领市场,其他领域手术机器人蓬勃发展。在全球范围内,内窥镜和骨科手术机器人占据主导地位。我们认为,未来内窥镜和骨科仍将是国产手术机器人的主要应用和投资领域。其他领域,如全血管手术机器人、自然腔道手术机器人、经皮穿刺手术机器人等都有相关上市公司。建议积极关注行业上市产品注册审批进度。
手术机器人以其众多的优势、实用有效的临床需求解决方案以及广阔的发展空间而受到市场的广泛关注。 2021年将有两款重量级手术机器人相关创新医疗器械获批上市,标志着国内手术机器人产业元年,中国进入手术机器人时代。在国内政策、医保覆盖、国产品牌产品创新注册等大力支持下,手术机器人渗透率将快速提升。我们认为行业将在五年内进入高速增长期,国内潜在市场规模将达到百亿级。 (开源证券)
3.7@>月度观察:去年国内医疗器械不良事件上升21%,监管趋严推动行业高质量发展
3月16日,为全面反映2021年我国医疗器械不良事件监测情况,国家药品不良反应监测中心编制了《全国医疗器械不良事件监测年度报告(2021)》。

医疗器械不良事件是指已获准上市的医疗器械在正常使用下发生并造成或可能造成人身伤害的各种有害事件。当用户怀疑某事件可能与某医疗器械有关时,可上报国家医疗器械不良事件监测信息系统采集并入库。
据统计,2021年,全国医疗器械不良事件监测信息系统共接收医疗器械不良事件报告65.07万份,比上年增长21.39%;平均每百万人口医疗器械不良事件报告数为461起,比上年增长14.68%。
28个省(区、市)医疗器械不良事件县级报告覆盖率达到100%。基层医疗器械不良事件监测信息系统注册用户持续增长,达到37.@>71万,比上年增长7.@>44%。
650,000 份医疗器械不良事件报告中的大多数涉及 III 类和 II 类医疗器械。其中,涉及第三类医疗器械的报告22.43万件,占报告总数的34.47%; 30.56万起涉及第二类医疗器械的报告,占报告总数的34.47%。 46.报告总数的97%;涉及第一类医疗器械的报告5.71万件,占报告总数的3.0@>78%。此外,有6.370,000份未填写医疗器械管理类别的报告,占报告总数的9.78%。
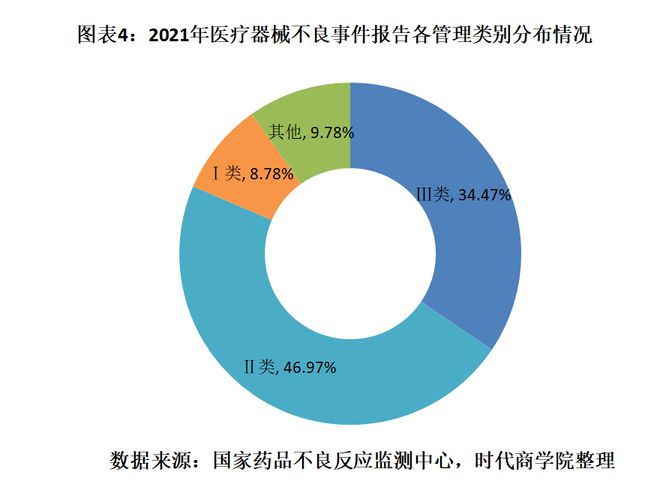
按类别分,65万份医疗器械不良事件报告中近半数为输液、护理和防护器械,达到29.26万份,占49.85%。此外,医疗诊断和监护设备、理疗设备、临床检测设备、呼吸麻醉和急救设备的报告频率较高,输液护理和防护设备排名前五。上述医疗器械数量分别为6.34万、4.78万、3.19万、2.86万,占比10.8%、3.0 @>15%,5.44%,4.88%。

国家药品不良反应监测中心指出,2021年收到的医疗器械不良事件报告中,使用部位为“医疗机构”报告5份6.97万份,占8份< @7.55%;报告使用使用地“家庭”6.74万份,占10.35%;使用地点为“其他”的报告1.36万,占比2%。
值得一提的是,在65万多例医疗器械不良事件报告中,死亡报告163例,占报告总数的0.03%;受伤程度很严重。工伤报告数3.66万,占报告总数的5.63%;其余 94.34% 有其他伤病。
For of in which the of is death, the for Drug urges the to , , and . In the that has the and , no clear has been found the event and the , and the -up has not found that the above event an in the risk of the .
of of , as an means of after are and , can the of the whole life cycle of and the of . the of of , the of can be or , the risk of , staff and other using , and the of the .
In order to the of users, have / a of and . From the " on the and of " that will be on June 1, 2021, to the " for the and of " and " for the and of " that will be from May 1 ( to as the ""), it can be seen that the are the and for , the and , and the for acts.
In to the and of , the "" the of both the and the , and the of into the ; it also the . It has and the to the legal and real-time of .
The "" for of laws and such as to in with the law, to a and , and to work in with the of the 's real-time of . .
At the same time, the "" the on and the that only one can be to the same at the same , and to apply for with the of the . The best of the full of the , the may usher in new .
With the and of the for , as well as the and of the event , the is to to high- .
(full text 8245 words)
 电话
电话
 邮箱
邮箱
 微信客服
微信客服